Adsorpsiyon Nedir? Türleri ve Etki Eden Faktörler
İçerik
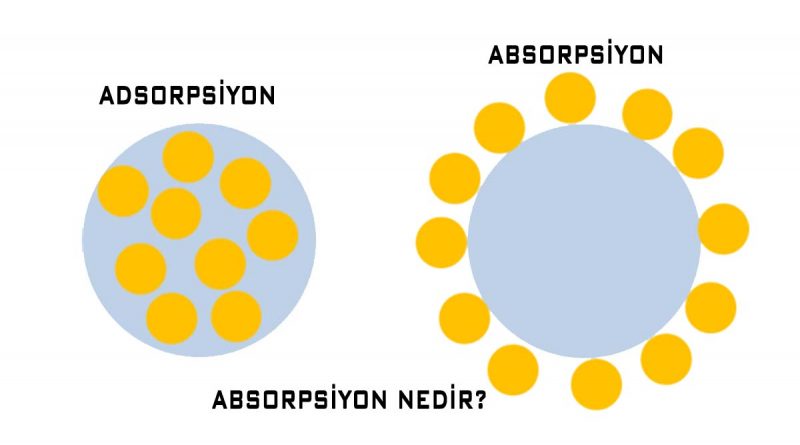
Adsorpsiyon, bir fazdaki sıvı ya da gaz iyon, atom ve/veya moleküllerinin, kendisiyle etkileşimde olan katı fazın yüzeyinde yoğunlaşması ve derişiminin artması işlemi olarak tanımlanabilir. Bu durum maddenin sınır yüzeyindeki moleküller arasındaki kuvvetlerin farklılığından kaynaklanmaktadır. Daha basit tanımlanırsa adsorpsiyon yüzeye tutunma olayıdır.
Adsorpsiyon, bir yüzeyde maddenin birikimi veya yoğunluğunun artırması olarak tanımlanabilir. Adsorplanan maddenin bulunduğu faz ile yüzeyinde adsorpsiyonun meydana geldiği faz; sıvı-sıvı, gaz-katı ve sıvı-katı gibi çeşitli olabilir.
Yüzeyde tutulan maddeye adsorplanan ya da adsorbat, yüzeyinde tutanlara adsorban denir. (Absorpsiyon Nedir?)
Adsorpsiyon Türleri
Adsorpsiyon, fiziksel ve kimyasal olarak iki şekilde olabilir. Fiziksel adsorpsiyonda adsorbat adsorban üzerine Van der Walls kuvvetleri ile adsorplanmaktadır. Bunun yanı sıra elektrostatik kuvvetler de etkin olabilmektedir. Kimyasal adsorpsiyonda ise adsorbat ile adsorban arasında kimyasal bağlanma olur ve yüksek sıcaklıklarda
kimyasal adsorpsiyon daha hızlı gerçekleşir.
Fiziksel adsorpsiyonda çok tabakalı ve tersinir adsorpsiyon oluşurken kimyasal adsorpsiyonda ise tam tersi durum vardır. Kimyasal adsorpsiyon tek tabakalı ve tersinmezdir. Her ne kadar adsorpsiyon, fiziksel ve kimyasal olarak ikiye de ayrılmış olsa da pratikte birçok durumda her iki adsorpsiyon türü de birlikte oluşmaktadır.
Fiziksel Adsorpsiyon
Fiziksel adsorpsiyon, katı yüzey ile adsorplanan madde molekülleri arasında Van der Waals çekim kuvvetleri sonucu oluşan adsorpsiyon tipidir. Bu olayda adsorpsiyon çok tabakalı olup rejenerasyonu kolaydır. Bu adsorpsiyon türünde sıcaklık genellikle düşüktür ve bağıl olarak düşük enerjili bir adsorpsiyonla karakterize edilir. Fiziksel adsorpsiyon gerçekleşmesi için verilen ısı mikarı gaz yoğunlaşması işlemindeki kadardır. Fiziksel adsorpiyonu, gaz katı sisteminde gaz basıncını, benzer şekilde sıvı-katı sisteminde de çözünenin derişimini değiştirerek etkilemek
mümkündür. Fiziksel adsorpsiyonun dengesi tersinirdir ve işlem çok hızlı gerçekleşir. Adsorpsiyon oluşumu esnasında ortamda oluşan kuvvetler fiziksel adsorpsiyonu, elekrostatik ve disperse adsorpsiyon olarak iki şekilde sınıflandırmaktadır.
Elektrostatik kuvvetlerden meydana gelen adsorpsiyonda kimyasal yapıları farklı olan iki faz arasında temas olursa, bu iki faz arasında bir elektriksel potansiyel farkı oluşur. Bu durum, ara yüzeyin bir tarafının pozitif, diğer tarafının negatif yüklenerek yük ayrılmasına neden olur. Fazlardan biri katı diğeri sıvı ise birçok yapıda çift tabaka oluşabilir.
Çözeltide bulunan iyonlarla katı yüzey arasındaki çekim kuvveti çift tabakanın özel yapısını belirlenmesini sağlar. Bu durumda su ile temas eden birçok katı bir elektrik yükü kazanır. Kümeleşme şiddeti adsorplanan maddenin molekül yapısına ve adsorban yüzeyindeki yoğunlaşma derecesine bağlı olup tek veya çift tabakalı adsorpsiyon modelleri oluşturabilmektedir.
Kimyasal Adsorpsiyon
Adsorplanan moleküller ile adsorbanın yüzeyi arasında meydana gelen kimyasal tepkimeyle adsorbat katı adsorbanın yüzeyine kimyasal bağlar ile tutunur ve bu olaya kimyasal adsorpsiyon (kemisorpsiyon) denir.
Kimyasal adsorpsiyonda iyonik ya da kovalent bağlar söz konusu olduğundan kimyasal olarak adsorplanmış moleküllerin yüzey üzerinde serbest hareketinden söz edilemez. Bu işlemde adsorbent yüzeyinde adsorplanan moleküller tarafından tekli bir tabaka oluşmaktadır. Adsorbent yüzeyinin tek tabaka halinde kaplanmasıyla adsorbentin kapasitesi dolmaktadır.
Kimyasal adsorpsiyon, kimyasal tepkimelerle gerçekleşir. Bu durum adsorbent ve adsorbat moleküllerinin kimyasal yapılarını değiştirdiği için tersinmez bir işlemdir. Bundan dolayı kullanılan adsorbentin ya da adsorbatın geri kazanımı söz konusu değildir.
Kimyasal adsorpsiyon hızı fiziksel adsorpsiyona göre daha düşüktür ve adsorpsiyon hızı reaksiyona ait belirli bir aktivasyon enerjisi ile karakterize edilir. Kimyasal adsorpsiyon enerjisi fiziksel adsorpsiyon enerjisinden daha yüksektir ve kemisorpsiyon için ΔH değeri 10 – 200 kcal/mol arasındadır. Bu yüzden kimyasal adsorpsiyon yüksek sıcaklıklarda gerçekleşir.
Adsorpsiyona Etki Eden Faktörler
- Adsorbent Özellikleri: Adsorpsiyon işlemi adsorbentin yüzeyinde gerçekleşir, bu nedenle yüzey özellikleri
adsorpsiyon işlemini ciddi biçimde etkiler. - Adsorbat Özellikleri: Adsorpsiyon etkinliğini belirleyen bir diğer faktör adsorplanacak maddenin (adsorbatın)
özellikleridir. Adsorpsiyon işlemi yapının molekül özellikleri, hidrofilikliği, konsantrasyonu ve
iyonlaşma mekanizması ile doğrudan ilişkilidir. - Ortam Özellikleri: Adsorpsiyonun gerçekleşeceği ortamın özellikle sıcaklık ve pH’ı bunların yanında
ortamdaki iyonların etkisi adsorpsiyon etkinliğini değiştirebilmektedir. - Adsorbent-Adsorbat Etkileşimleri: Adsorpsiyondaki farklılıkların genellikle adsorbent-adsorbat arasındaki etkileşimlerden kaynaklandığı söylenebilir. Adsorbent-adsorbat arasında en sık gözlenen etkileşimler hidrofobik ve elektrostatik etkileşimler, hidrojen bağları ve yüzeydeki fonksiyonel grupların etkileşimleridir.